- las atracciones moleculares son más débiles que los enlaces covalentes porque no son el resultado de compartir pares de electrones entre átomos; es decir, son interacciones no covalentes: fuerzas de atracción que no son enlaces iónicos y que son diferentes de los enlaces covalentes. Las interacciones no covalentes entre moléculas (fuerzas intermoleculares) explican el punto de fusión, el punto de ebullición y otras propiedades de las sustancias que no son iónicas. Las interacciones no covalentes entre diferentes partes de una molécula grande (fuerzas intramoleculares) mantienen las moléculas de importancia biológica con la forma exacta que requieren para desempeñar sus funciones. Por ejemplo, un gran número de interacciones no covalentes entre las cadenas de ADN establecen la estructura de doble hélice de esta molécula de gran tamaño. Sin embargo, las interacciones no covalentes individuales dentro del ADN son bastante débiles como para que sean vencidas en condiciones fisiológicas, lo cual hace posible la separación de las dos cadenas del ADN para copiarlos.
Estados De Agregación De La Materia
jueves, 13 de junio de 2013
fuerza de atracción entre moleculas
líquidos y solidos
LIQUIDO
El estado líquido es un estado de agregación de la materia intermedio entre el estado solido y el estado gaseoso. Las moleculas de los líquidos no están tan próximas como las de los sólidos, pero están menos separadas que las de los gases. Las moléculas en el estado líquido ocupan posiciones al azar que varían con el tiempo. Las distancias intermoleculares son constantes dentro de un estrecho margen. En algunos líquidos, las moléculas tienen una orientación preferente, lo que hace que el líquido presente propiedades anistropas(propiedades, como el indice de refacción , que varían según la dirección dentro del material).
Los líquidos presentan tensión superficial y capilaridad, generalmente se dilatan cuando se incrementa su temperatura y pierden volumen cuando se enfrían, aunque sometidos a compresión su volumen es muy poco variable a diferencia de lo que sucede con otros fluidos como los gases. Los objetos inmersos en algún líquido están sujetos a un fenómeno conocido como flotabilidad.
SOLIDO
Un cuerpo sólido es uno de los cuatro estados de agregación de la materia (siendo los otros gas, líquido, Plasma y el Bose-Einstein), se caracteriza porque opone resistencia a cambios de forma y de volumen. Sus partículas se encuentran juntas y correctamente ordenadas. Las moléculas de un sólido tienen una gran cohesión y adoptan formas bien definidas. Existen varias disciplinas que estudian los sólidos:
- La física del estado sólido estudia de manera experimental y teórica la materia condensada, es decir, de líquidos y sólidos que contengan más de 1019 átomos en contacto entre sí
- La mecánica de sólidos deformables estudia propiedades microscópicas desde la perspectiva de la mecánica de medios continuos (tensión, deformación, magnitudes termodinámicas, &c.) e ignora la estructura atómica interna porque para cierto tipo de problemas esta no es relevante.
- La ciencia de los materiales se ocupa principalmente de propiedades de los sólidos como estructura y transformaciones de fase.
- La química del estado sólido se especializa en la síntesis de nuevos materiales.
Manteniendo constante la presión a baja temperatura los cuerpos se presentan en forma sólida y encontrándose entrelazados formando generalmente estructuras cristalinas. Esto confiere al cuerpo la capacidad de soportar fuerzas sin deformación aparente. Son, por tanto, agregados generalmente rígidos, incompresibles (que no pueden ser comprimidos), duros y resistentes. Poseen volumen constante y no se difunden, ya que no pueden desplazarse.
estado plasma y superfluidos
PLASMA
el plasma es el cuarto estado de la materia.los otros tres solido,liquido y gaseoso.
En la mayoría de los casos, la materia en la tierra tiene electrones que orbitan alrededor del núcleo del átomo. Los electrones que tienen carga negativa son atraídos hacia el núcleo de carga positiva. ¡Recuerda, los opuestos se atraen!, por lo que los electrones se quedan orbitando alrededor del núcleo. Cuando la temperatura es muy elevada los electrones pueden escapar de sus órbitas alrededor del núcleo del átomo. Cuando el electrón(es) se vá(n), eso deja lo que los científicos llaman un ión de carga positiva. Este proceso es similar al de una nave espacial cuando escapa de la fuerza de gravedad de la Tierra.
En resumen, cuando los electrones ya no están atrapados en sus órbitas alrededor del núcleo, tenemos el estado de plasma. Esto es cuando un gas se convierte en un montón de electrones que se han escapado de la fuerza del núcleo y los iones que están cargados positivamente porque han perdido uno o más electrones.
SUPERFLUIDOS
El superfluido (también llamado Condensado de Bose-Einstein) es un estado de la materia caracterizado por la ausencia total de viscosidad (lo cual lo diferencia de una sustancia muy fluida, la cual tendría una viscosidad próxima a cero, pero no exactamente igual a cero), de manera que, en un circuito cerrado, fluiría interminablemente sin fricción. Fue descubierta en 1937 por Pyotr Leonidovich Kapitsa, John F. Allen y Don Misener, y a su estudio se lo llama hidrodinámica cuántica.
Es un fenómeno físico que tiene lugar a muy bajas temperaturas, cerca del cero absoluto, límite en el que cesa toda actividad. Un inconveniente es que casi todos los elementos se congelan a esas temperaturas. Pero hay una excepción: el helio. Existen dos isótopos estables del helio, el helio-4 (que es muy común) y el helio-3 (que es raro) y se produce en la desintegración beta del tritio en reactores nucleares. También se encuentra en la superficie de la Luna, arrastrado hasta allí por el viento solar.
Los dos isótopos se comportan de modos muy diferentes, lo cual sirve para examinar los efectos de las dos estadísticas cuánticas, la estadística de Fermi-Dirac, a la que obedecen las partículas de espín semi-entero, y la estadística de Bose-Einstein, seguida por las partículas de espín entero.
Una característica del superfluido es que pueden atravesar cualquier objeto sólido o cualquier superficie no porosa, debido a su fuerte capacidad de oscilación, característica que demuestra los argumentos de Física Cuántica en contra de los de Albert Einstein.
el plasma es el cuarto estado de la materia.los otros tres solido,liquido y gaseoso.
En la mayoría de los casos, la materia en la tierra tiene electrones que orbitan alrededor del núcleo del átomo. Los electrones que tienen carga negativa son atraídos hacia el núcleo de carga positiva. ¡Recuerda, los opuestos se atraen!, por lo que los electrones se quedan orbitando alrededor del núcleo. Cuando la temperatura es muy elevada los electrones pueden escapar de sus órbitas alrededor del núcleo del átomo. Cuando el electrón(es) se vá(n), eso deja lo que los científicos llaman un ión de carga positiva. Este proceso es similar al de una nave espacial cuando escapa de la fuerza de gravedad de la Tierra.
En resumen, cuando los electrones ya no están atrapados en sus órbitas alrededor del núcleo, tenemos el estado de plasma. Esto es cuando un gas se convierte en un montón de electrones que se han escapado de la fuerza del núcleo y los iones que están cargados positivamente porque han perdido uno o más electrones.
SUPERFLUIDOS
El superfluido (también llamado Condensado de Bose-Einstein) es un estado de la materia caracterizado por la ausencia total de viscosidad (lo cual lo diferencia de una sustancia muy fluida, la cual tendría una viscosidad próxima a cero, pero no exactamente igual a cero), de manera que, en un circuito cerrado, fluiría interminablemente sin fricción. Fue descubierta en 1937 por Pyotr Leonidovich Kapitsa, John F. Allen y Don Misener, y a su estudio se lo llama hidrodinámica cuántica.
Es un fenómeno físico que tiene lugar a muy bajas temperaturas, cerca del cero absoluto, límite en el que cesa toda actividad. Un inconveniente es que casi todos los elementos se congelan a esas temperaturas. Pero hay una excepción: el helio. Existen dos isótopos estables del helio, el helio-4 (que es muy común) y el helio-3 (que es raro) y se produce en la desintegración beta del tritio en reactores nucleares. También se encuentra en la superficie de la Luna, arrastrado hasta allí por el viento solar.
Los dos isótopos se comportan de modos muy diferentes, lo cual sirve para examinar los efectos de las dos estadísticas cuánticas, la estadística de Fermi-Dirac, a la que obedecen las partículas de espín semi-entero, y la estadística de Bose-Einstein, seguida por las partículas de espín entero.
Una característica del superfluido es que pueden atravesar cualquier objeto sólido o cualquier superficie no porosa, debido a su fuerte capacidad de oscilación, característica que demuestra los argumentos de Física Cuántica en contra de los de Albert Einstein.
los gases y sus propiedades
Los gases son fluidosaltamente compresibles, que experimentan grandes cambios de densidad con la presión y la temperatura. Las moléculas que constituyen un gas casi no son atraídas unas por otras, por lo que se mueven en el vacío a gran velocidad y muy separadas unas de otras, explicando así las propiedades:
- Las moléculas de un gas se encuentran prácticamente libres, de modo que son capaces de distribuirse por todo el espacio en el cual son contenidos. Las fuerzas gravitatorias y de atracción entre las moléculas son despreciables, en comparación con la velocidad a que se mueven las moléculas.
- Los gases ocupan completamente el volumen del recipiente que los contiene.
- Los gases no tienen forma definida, adoptando la de los recipientes que las contiene.
- Pueden comprimirse fácilmente, debido a que existen enormes espacios vacíos entre unas moléculas y otras.
A temperatura y presión ambientales los gases pueden ser elementos como el hidrógeno, el oxígeno el nitrógeno el cloro el flúor y los gases nobles, compuestos como el dióxido de carbono o el propano, o mezclas como el aire.
Los vapores y el plasma comparten propiedades con los gases y pueden formar mezclas homogéneas , por ejemplo vapor de agua yaire, en conjunto son conocidos como cuerpos gaseosos, estado gaseoso o fase gaseosa.
Las particulas de gas están en continuo movimiento en dirección aleatoria y con frecuencia chocan unas con otras. Las colisiones entre las partículas son perfectamente elásticas, es decir, la energía se transfiere de una partícula a otra por efecto de las colisiones; sin embargo, la energía total de todas las partículas del sistema permanece inalterada.
La energía cinética promedio de las partículas es proporcional a la temperatura del gas (en Kelvin), la energía cinética promedio de una partícula
ecuaciones del comportamiento de los gases
 |
La ecuación que describe normalmente la relación entre la presión, el volumen, la temperatura y la cantidad (en moles) de un gas ideal es:
Donde:
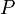 = presion absoluta
= presion absoluta = Volumen
= Volumen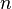 = Moles de gas
= Moles de gas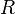 = constante universal de los gases ideales
= constante universal de los gases ideales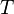 = Temperatura absoluta
= Temperatura absoluta
Teoría cinética molecula
Esta teoría fue desarrollada por Ludwith Boltzmann y Maxwell. Nos indica las propiedades de un gas ideal a nivel molecular.
- Todo gas ideal está formado por N pequeñas partículas puntuales (átomos o moléculas).
- Las moléculas gaseosas se mueven a altas velocidades, en forma recta y desordenada.
- Un gas ideal ejerce una presión continua sobre las paredes del recipiente que lo contiene, debido a los choques de las partículas con las paredes de este.
- Los choques moleculares son perfectamente elásticos. No hay pérdida de energía cinética.
- No se tienen en cuenta las interacciones de atracción y repulsión molecular.
- La energis cinetica media de la translación de una molécula es directamente proporcional a la temperatura absoluta del gas.
En estas circunstancias, la ecuación de los gases se encuentra teóricamente:
Suscribirse a:
Entradas (Atom)


.jpg)

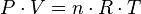

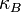 es la constante de
es la constante de